Peptiidid on ühendite klass, mis moodustuvad mitme aminohappe ühendamisel peptiidsidemete kaudu.Nad on elusorganismides üldlevinud.Siiani on elusorganismidest leitud kümneid tuhandeid peptiide.Peptiidid mängivad olulist rolli erinevate süsteemide, organite, kudede ja rakkude funktsionaalse tegevuse reguleerimisel ning elutegevuses ning neid kasutatakse sageli funktsionaalanalüüsis, antikehade uurimisel, ravimite väljatöötamisel ja muudes valdkondades.Biotehnoloogia ja peptiidide sünteesi tehnoloogia arenedes on üha rohkem peptiidravimeid välja töötatud ja kliinikus rakendatud.
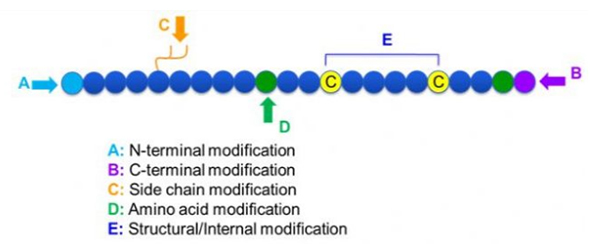
Peptiidide modifikatsioone on väga erinevaid, mida saab lihtsalt jagada modifikatsioonijärgseteks ja protsessi modifikatsioonideks (kasutades tuletatud aminohappe modifikatsiooni) ning N-terminaalseks modifikatsiooniks, C-terminaalseks modifikatsiooniks, kõrvalahela modifikatsiooniks, aminohappe modifikatsiooniks, skeleti modifikatsiooniks, jne, olenevalt muutmiskohast (joonis 1).Olulise vahendina peptiidahelate peamise ahela struktuuri või kõrvalahelarühmade muutmisel võib peptiidide modifitseerimine tõhusalt muuta peptiidühendite füüsikalisi ja keemilisi omadusi, suurendada vees lahustuvust, pikendada toimeaega in vivo, muuta nende bioloogilist jaotumist, kõrvaldada immunogeensust. , vähendada toksilisi kõrvalmõjusid jne. Selles artiklis tutvustatakse mitmeid peamisi peptiidide modifitseerimise strateegiaid ja nende omadusi.
1. Tsükliseerimine
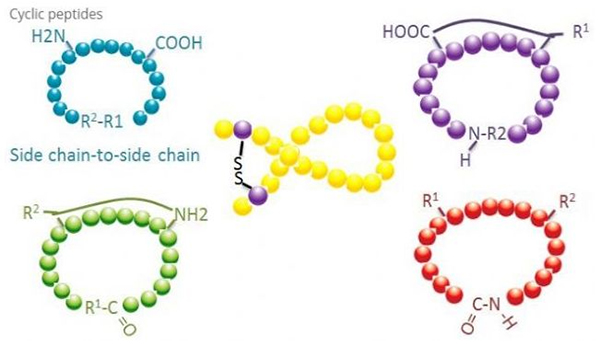
Tsüklilistele peptiididele on biomeditsiinis palju rakendusi ja paljud bioloogilise aktiivsusega looduslikud peptiidid on tsüklilised peptiidid.Kuna tsüklilised peptiidid kipuvad olema jäigemad kui lineaarsed peptiidid, on nad seedesüsteemi suhtes äärmiselt vastupidavad, võivad seedetraktis ellu jääda ja neil on suurem afiinsus sihtretseptorite suhtes.Tsükliseerimine on kõige otsesem viis tsükliliste peptiidide sünteesimiseks, eriti suure struktuurse skeletiga peptiidide puhul.Tsükliseerimisrežiimi järgi saab selle jagada külgahela küljeahela tüübiks, klemm - külgahela tüübiks, terminali tüübiks (otsast lõpuni tüüp).
(1) külgahelast külgahelasse
Kõige tavalisem külgahelast külgahelasse tsüklistamise tüüp on tsüsteiinijääkide vaheline disulfiidsild.See tsüklistamine viiakse sisse tsüsteiinijääkide paariga, mille kaitse eemaldatakse ja seejärel oksüdeeritakse, moodustades disulfiidsidemeid.Polütsüklilise sünteesi saab saavutada sulfhüdrüülkaitserühmade selektiivse eemaldamisega.Tsükliseerimist saab teha kas dissotsiatsioonijärgses lahustis või dissotsiatsioonieelsel vaigul.Tsükliseerimine vaikudel võib olla vähem efektiivne kui lahustiga tsüklistamine, kuna vaikudel olevad peptiidid ei moodusta kergesti tsüklistatud konformatsioone.Teine külgahela külgahela tsüklistamise tüüp on amiidi struktuuri moodustamine asparagiinhappe või glutamiinhappe jäägi ja aluselise aminohappe vahel, mis eeldab, et külgahela kaitserühma peab olema võimalik polüpeptiidist selektiivselt eemaldada. vaigul või pärast dissotsiatsiooni.Kolmas külgahela - külgahela tsüklistamise tüüp on difenüüleetrite moodustamine türosiini või p-hüdroksüfenüülglütsiini abil.Seda tüüpi tsüklistamist looduslikes toodetes leidub ainult mikroobsetes toodetes ja tsüklisatsioonitoodetel on sageli potentsiaalne raviväärtus.Nende ühendite valmistamine nõuab ainulaadseid reaktsioonitingimusi, mistõttu neid tavaliste peptiidide sünteesil sageli ei kasutata.
(2) terminalist külgahelani
Terminaalse külgahela tsüklistamine hõlmab tavaliselt C-otsa lüsiini või ornitiini kõrvalahela aminorühmaga või N-otsa asparagiinhappe või glutamiinhappe kõrvalahelaga.Muu polüpeptiidi tsüklistamine toimub eetersidemete moodustamisega C-terminaalse ja seriini või treoniini kõrvalahelate vahel.
(3) Terminal või pea-saba tüüp
Ahelpolüpeptiide saab kas tsüklistada lahustis või kinnitada vaigule külgahela tsüklimise teel.Peptiidide oligomeriseerumise vältimiseks tuleks lahusti tsentraliseerimisel kasutada peptiidide madalaid kontsentratsioone.Pea-saba sünteetilise ringpolüpeptiidi saagis sõltub ahela polüpeptiidi järjestusest.Seetõttu tuleks enne tsükliliste peptiidide suuremahulist valmistamist esmalt luua võimalike aheldatud juhtpeptiidide raamatukogu, millele järgneb tsüklistamine, et leida parimate tulemustega järjestus.
2. N-metüülimine
N-metüülimine toimub algselt looduslikes peptiidides ja see viiakse peptiidide sünteesi, et vältida vesiniksidemete moodustumist, muutes seeläbi peptiidid biolagunemise ja kliirensi suhtes vastupidavamaks.Peptiidide süntees N-metüülitud aminohappe derivaatide abil on kõige olulisem meetod.Lisaks võib kasutada ka N-(2-nitrobenseensulfonüülkloriid) polüpeptiid-vaigu vaheühendite Mitsunobu reaktsiooni metanooliga.Seda meetodit on kasutatud N-metüülitud aminohappeid sisaldavate tsükliliste peptiidide raamatukogude valmistamiseks.
3. Fosforüülimine
Fosforüülimine on üks levinumaid translatsioonijärgseid modifikatsioone looduses.Inimese rakkudes on üle 30% valkudest fosforüülitud.Fosforüülimine, eriti pöörduv fosforüülimine, mängib olulist rolli paljude rakuliste protsesside, näiteks signaaliülekande, geeniekspressiooni, rakutsükli ja tsütoskeleti regulatsiooni ning apoptoosi kontrollimisel.
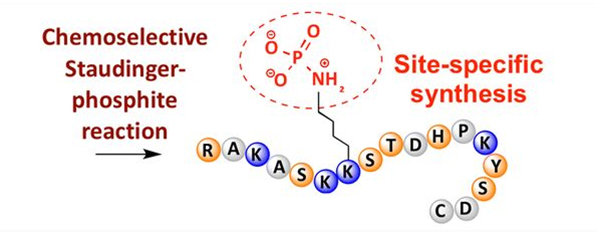
Fosforüülimist võib täheldada mitmesuguste aminohappejääkide juures, kuid kõige levinumad fosforüülimise sihtmärgid on seriini-, treoniini- ja türosiinijäägid.Fosfotürosiini, fosfotreoniini ja fosfoseriini derivaate võib sisestada peptiididesse sünteesi ajal või moodustada pärast peptiidide sünteesi.Selektiivset fosforüülimist saab saavutada seriini, treoniini ja türosiini jääkide abil, mis eemaldavad selektiivselt kaitserühmad.Mõned fosforüülimisreagendid võivad polüpeptiididesse viia ka fosforhapperühmi järelmodifikatsiooni teel.Viimastel aastatel on lüsiini kohaspetsiifiline fosforüülimine saavutatud keemiliselt selektiivse Staudingeri-fosfiidi reaktsiooni abil (joonis 3).
4. Müristoüülimine ja palmitoüülimine
N-terminali atsüülimine rasvhapetega võimaldab peptiididel või valkudel seonduda rakumembraanidega.N-otsa müridamoüülitud järjestus võimaldab Src perekonna proteiinkinaasidel ja pöördtranskriptaasi Gaq valkudel suunata rakumembraanidega seonduma.Müristiinhape ühendati vaik-polüpeptiidi N-otsaga, kasutades standardseid sidestusreaktsioone, ning saadud lipopeptiidi võis standardtingimustes dissotsieerida ja puhastada RP-HPLC-ga.
5. Glükosüülimine
Glükopeptiidid, nagu vankomütsiin ja teikolaniin, on olulised antibiootikumid ravimiresistentsete bakteriaalsete infektsioonide raviks ning immuunsüsteemi stimuleerimiseks kasutatakse sageli teisi glükopeptiide.Lisaks, kuna paljud mikroobsed antigeenid on glükosüülitud, on väga oluline uurida glükopeptiide, et parandada infektsiooni terapeutilist toimet.Teisest küljest on leitud, et kasvajarakkude rakumembraanil olevad valgud näitavad ebanormaalset glükosüülimist, mistõttu glükopeptiidid mängivad olulist rolli vähi ja kasvaja immuunkaitseuuringutes.Glükopeptiide valmistatakse Fmoc/t-Bu meetodil.Glükosüülitud aminohappeid kaitsvad pentafluorofenoolestriga aktiveeritud fMOC-d sisestatakse polüpeptiididesse sageli glükosüülitud jääke, nagu treoniin ja seriin.
6. Isopreen
Isopentadienüülimine toimub tsüsteiini jääkides külgahelas C-terminali lähedal.Valgu isopreen võib parandada rakumembraani afiinsust ja moodustada valgu-valgu interaktsiooni.Isopentadieneeritud valkude hulka kuuluvad türosiinfosfataas, väike GTaas, košaperooni molekulid, tuumakiht ja tsentromeersed sidumisvalgud.Isopreenpolüpeptiide saab valmistada, kasutades isopreeni vaikudel või lisades tsüsteiini derivaate.
7. Polüetüleenglükooli (PEG) modifikatsioon
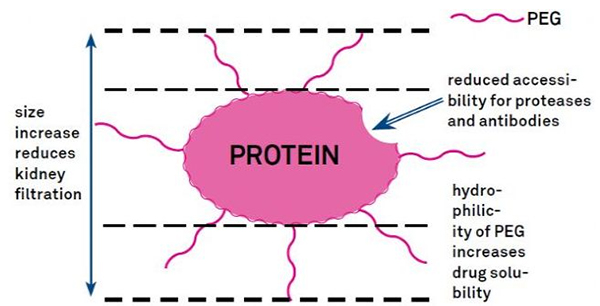
PEG modifikatsiooni saab kasutada valgu hüdrolüütilise stabiilsuse, biojaotumise ja peptiidide lahustuvuse parandamiseks.PEG-ahelate sisestamine peptiididesse võib parandada nende farmakoloogilisi omadusi ja inhibeerida ka peptiidide hüdrolüüsi proteolüütiliste ensüümide poolt.PEG-peptiidid läbivad glomerulaarkapillaaride ristlõiget kergemini kui tavalised peptiidid, vähendades oluliselt renaalset kliirensit.PEG-peptiidide pikema aktiivse poolväärtusaja tõttu in vivo saab normaalset ravitaset säilitada väiksemate annuste ja harvemate peptiidravimitega.Kuid PEG-i modifikatsioonil on ka negatiivseid mõjusid.Suured kogused PEG-i takistavad ensüümil peptiidi lagundamast ja vähendavad ka peptiidi seondumist sihtretseptoriga.Kuid PEG-peptiidide madalat afiinsust kompenseerib tavaliselt nende pikem farmakokineetiline poolväärtusaeg ja kuna PEG-peptiidid on kehas kauem olemas, on PEG-peptiididel suurem tõenäosus sihtkudedesse imenduda.Seetõttu tuleks optimaalsete tulemuste saavutamiseks optimeerida PEG-polümeeri spetsifikatsioonid.Teisest küljest kogunevad PEG-peptiidid maksa vähenenud renaalse kliirensi tõttu, mille tulemuseks on makromolekulaarne sündroom.Seetõttu tuleb ravimite testimisel peptiide kasutades PEG-i modifikatsioone hoolikamalt kavandada.
PEG modifikaatorite tavalised modifikatsioonirühmad võib kokku võtta järgmiselt: amino (-amiin) -NH2, aminometüül-Ch2-NH2, hüdroksü-OH, karboksü-Cooh, sulfhüdrüül (-tiool) -SH, maleimiid -MAL, suktsiinimiidkarbonaat - SC, suktsiinimiidatsetaat -SCM, suktsiinimiidpropionaat -SPA, n-hüdroksüsuktsiinimiid -NHS, akrülaat-ch2ch2cooh, aldehüüd -CHO (nagu propioonald, butüürALD), akrüülalus (-akrülaat-akrl), bioasidüülasiid, Biotiin, fluorestseiin, glutarüül-GA, akrülaathüdrasiid, alküün-alküün, p-tolueensulfonaat-OT-d, suktsinimiidsuktsinaat -SS jne. PEG-i derivaadid karboksüülhapetega võivad olla sidestatud n-terminaalsete amiinide või lüsiini kõrvalahelatega.Aminoaktiveeritud PEG võib olla seotud asparagiinhappe või glutamiinhappe kõrvalahelatega.Mal-aktiveeritud PEG-i saab konjugeerida täielikult deprotekteeritud tsüsteiini kõrvalahelate merkaptaaniga [11].PEG modifikaatorid klassifitseeritakse tavaliselt järgmiselt (märkus: mPEG on metoksü-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) sirge ahelaga PEG modifikaator
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OT, mPEG-SH, mPEG-ALD, mPEG-butüürALD, mPEG-SS
(2) bifunktsionaalne PEG modifikaator
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) hargnev PEG modifikaator
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotiniseerimine
Biotiin võib olla tugevalt seotud avidiini või streptavidiiniga ning seondumistugevus on isegi lähedane kovalentsele sidemele.Biotiiniga märgistatud peptiide kasutatakse tavaliselt immuunanalüüsis, histotsütokeemias ja fluorestsentsil põhinevas voolutsütomeetrias.Märgistatud antibiotiini antikehi saab kasutada ka biotinüülitud peptiidide sidumiseks.Biotiini märgised on sageli kinnitatud lüsiini kõrvalahela või N-terminali külge.6-aminokaproonhapet kasutatakse sageli peptiidide ja biotiini vahelise sidemena.Side on substraadiga seondumisel paindlik ja seob paremini steeriliste takistuste olemasolul.
9. Fluorestseeruv märgistus
Fluorestsentsmärgistust saab kasutada polüpeptiidide jälgimiseks elusrakkudes ning ensüümide ja toimemehhanismide uurimiseks.Trüptofaan (Trp) on fluorestseeruv, seega saab seda kasutada olemuslikuks märgistamiseks.Trüptofaani emissioonispekter sõltub perifeersest keskkonnast ja väheneb lahusti polaarsuse vähenemisega – omadus, mis on kasulik peptiidi struktuuri ja retseptoriga seondumise tuvastamiseks.Trüptofaani fluorestsentsi saab kustutada protoneeritud asparagiinhappe ja glutamiinhappega, mis võib selle kasutamist piirata.Dansüülkloriidrühm (Dansyl) on aminorühmaga seotuna tugevalt fluorestseeruv ja seda kasutatakse sageli aminohapete või valkude fluorestseeruva märgisena.
Fluorestsentsresonants Energia muundamine (FRET) on kasulik ensüümiuuringute jaoks.FRET-i kasutamisel sisaldab substraadi polüpeptiid tavaliselt fluorestsentsi märgistavat rühma ja fluorestsentsi kustutavat rühma.Märgistatud fluorestseeruvad rühmad kustutatakse kustutajaga mittefotoonenergia ülekande kaudu.Kui peptiid on kõnealusest ensüümist dissotsieerunud, kiirgab märgistusrühm fluorestsentsi.
10. Puuri polüpeptiidid
Puuripeptiididel on optiliselt eemaldatavad kaitserühmad, mis kaitsevad peptiidi retseptoriga seondumise eest.UV-kiirgusega kokkupuutel peptiid aktiveerub, taastades oma afiinsuse retseptori suhtes.Kuna seda optilist aktiveerimist saab juhtida vastavalt ajale, amplituudile või asukohale, saab puuri peptiide kasutada rakkudes toimuvate reaktsioonide uurimiseks.Kõige sagedamini kasutatavad puuripolüpeptiidide kaitserühmad on 2-nitrobensüülrühmad ja nende derivaadid, mida saab peptiidide sünteesis sisestada kaitsvate aminohapete derivaatide kaudu.Aminohapete derivaadid, mis on välja töötatud, on lüsiin, tsüsteiin, seriin ja türosiin.Aspartaadi ja glutamaadi derivaate aga tavaliselt ei kasutata, kuna need on peptiidide sünteesi ja dissotsiatsiooni ajal vastuvõtlikud tsükliseerumisele.
11. Polüantigeenne peptiid (MAP)
Lühikesed peptiidid ei ole tavaliselt immuunsed ja antikehade tootmiseks tuleb need siduda kandevalkudega.Polüantigeenne peptiid (MAP) koosneb mitmest identsest peptiidist, mis on ühendatud lüsiini tuumadega, mis võivad spetsiifiliselt ekspresseerida suure potentsiaaliga immunogeene ja mida saab kasutada peptiidi-kandja valgu paaride valmistamiseks.MAP polüpeptiide saab sünteesida tahke faasi sünteesi teel MAP vaigul.Kuid mittetäieliku sidumise tulemuseks on peptiidahelate puudumine või kärbimine mõnel harul ja seega ei esine sellel algse MAP polüpeptiidi omadusi.Alternatiivina võib peptiide valmistada ja puhastada eraldi ning seejärel siduda MAP-ga.Peptiidisüdamiku külge kinnitatud peptiidjärjestus on hästi määratletud ja kergesti iseloomustatav massispektromeetria abil.
Järeldus
Peptiidide modifitseerimine on peptiidide kujundamise oluline vahend.Keemiliselt modifitseeritud peptiidid ei suuda mitte ainult säilitada kõrget bioloogilist aktiivsust, vaid ka tõhusalt vältida immunogeensuse ja toksilisuse puudusi.Samal ajal võib keemiline modifitseerimine anda peptiididele mõned uued suurepärased omadused.Viimastel aastatel on kiiresti arendatud CH aktiveerimise meetodit polüpeptiidide järelmodifikatsiooniks ning saavutatud on palju olulisi tulemusi.
Postitusaeg: 20. märts 2023
